UP Board and NCERT Solution of Class 10 Science [विज्ञान] ईकाई 1 रासायनिक पदार्थ- प्रकृति एवं व्यवहार – Chapter- 1 Chemical Reactions and Equations (रासायनिक अभिक्रियाएं एवं समीकरण) अतिलघु उत्तरीय प्रश्न एवं लघु उत्तरीय प्रश्न
प्रिय पाठक! इस पोस्ट के माध्यम से हम आपको कक्षा 10वीं विज्ञान ईकाई 1 रासायनिक पदार्थ- प्रकृति एवं व्यवहार (Chemical substances- Nature and Behavior ) के अंतर्गत चैप्टर 1 Chemical Reactions and Equations (रासायनिक अभिक्रियाएं एवं समीकरण) पाठ के अतिलघु उत्तरीय प्रश्न एवं लघु उत्तरीय प्रश्न प्रदान कर रहे हैं। UP Board आधारित प्रश्न हैं। आशा करते हैं हमारी मेहनत की क़द्र करते हुए इसे अपने मित्रों में शेयर जरुर करेंगे।

रासायनिक अभिक्रियाएँ- रासायनिक समीकरण, संतुलित रासायनिक समीकरण, संतुलित रासायनिक समीकरण का तात्पर्य, संतुलित रासायनिक अभिक्रियाओं के प्रकार- संयोजन अभिक्रिया, अपघटन (वियोजन) अभिक्रिया, विस्थापन अभिक्रिया, द्विविस्थापन अभिक्रिया, अवक्षेपण अभिक्रिया, उदासीनीकरण, उपचयन तथा अपचयन अभिक्रिया आदि पाठ्यक्रम के टॉपिक हैं।
| Class | 10th | Subject | Science (Vigyan) |
| Pattern | NCERT | Chapter- | Chemical Reactions and Equations |
अतिलघु उत्तरीय प्रश्न
प्रश्न 1.निम्नलिखित रासायनिक समीकरण को संतुलित कीजिए-
Fe (s) + H₂O (g) → Fe3 o4(s) + H₂(g)
उत्तर- संतुलित समीकरण
3Fe (s) + 4H2O (g) → Fe3O₄(s) + 2H₂ (g) 4
प्रश्न 2. आलू चिप्स निर्माता द्वारा चिप्स के पैकेट में कौन-सी गैस भरी जाती है?
उत्तर- आलू चिप्स निर्माता चिप्स के पैकेट में नाइट्रोजन गैस भरते हैं।
प्रश्न 3. संयोजन अभिक्रिया किसे कहते हैं?
उत्तर- वह रासायनिक अभिक्रिया, जिसमें दो या दो से अधिक पदार्थ (तत्त्व या यौगिक) संयोग करके एकल उत्पाद का निर्माण करते हैं, संयोजन अभिक्रिया कहलाती है।
उदाहरण- लोहा एवं गन्धक परस्पर गर्म करने पर आयरन सल्फाइड बनाते हैं।

प्रश्न 4.लोहे की कील को कॉपर सल्फेट के विलयन में डुबाने पर दिखाई देने वाले दो प्रेक्षणों को लिखिए। रासायनिक अभिक्रिया का समीकरण भी लिखिए।
अथवा
कॉपर सल्फेट विलयन में लोहे की कीलों को 30 मिनट तक डुबाए रखने के पश्चात् आप कीलों तथा कॉपर सल्फेट के रंग में क्या परिवर्तन देखते हैं?
उत्तर- जब लोहे की कील को कॉपर सल्फेट के विलयन में लगभग आधे घण्टे रखने के बाद देखते हैं तो कॉपर सल्फेट विलयन का गहरा नीला रंग, फेरस सल्फेट का हल्का हरा विलयन बनने के कारण लुप्त हो जाता है तथा लोहे की कील पर कॉपर धातु की लाल-भूरी परत जम जाती है। यह विस्थापन अभिक्रिया के कारण होता है-
![]()
प्रश्न 5. श्वसन को ऊष्माक्षेपी अभिक्रिया क्यों कहते हैं? कारण बताइए।
उत्तर- श्वसन के दौरान हमारे शरीर की कोशिकाओं में खाद्य पदार्थों के रूप में उपस्थित ग्लूकोस, ऑक्सीजन से संयोग करके CO, तथा H₂O के साथ-साथ ऊर्जा भी उत्सर्जित करता है।
![]()
चूंकि इस प्रक्रिया के दौरान ऊर्जा उत्पन्न होती है इसलिए श्वसन एक ऊष्माक्षेपी प्रक्रिया है।
प्रश्न 6.मैग्नीशियम रिबन को वायु में जलाने से पूर्व साफ करना चाहिए। क्यों?
उत्तर- मैग्नीशियम रिबन की सतह पर प्रायः बेसिक मैग्नीशियम कार्बोनेट (मैग्नीशियम कार्बोनेट और मैग्नीशियम हाइड्रॉक्साइड का मिश्रण) की रक्षी परत होती है। अतः मैग्नीशियम रिबन की सतह से बेसिक मैग्नीशियम कार्बोनेट की इस रक्षी परत को हटाने के लिए वायु में जलाने से पूर्व मैग्नीशियम रिबन या फीते को रेगमाल से रगड़कर साफ करना आवश्यक है। इससे मैग्नीशियम वायु के सीधे सम्पर्क में आ जाती है।
प्रश्न 7. भौतिक परिवर्तन तथा रासायनिक परिवर्तन में एक मुख्य अन्तर बताइए।
उत्तर- भौतिक परिवर्तन में कोई नया पदार्थ नहीं बनता है जबकि रासायनिक परिवर्तन में नया पदार्थ बनता है।
प्रश्न 8. अभिक्रिया CuO + H₂ → Cu + H₂O में किस पदार्थ का ऑक्सीकरण एवं किस पदार्थ का अपचयन हो रहा है? इस प्रकार की अभिक्रिया का एक अन्य उदाहरण दीजिए।
उत्तर-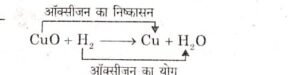
अतः स्पष्ट है कि (i) CuO में ऑक्सीजन निकल रही है अतः CuO का Cu में अपचयन हो रहा है। (ii) हाइड्रोजन से ऑक्सीजन का संयोग हो रहा है अतः H2 का जल (H₂O) में ऑक्सीकरण हो रहा है।
अन्य उदाहरण- 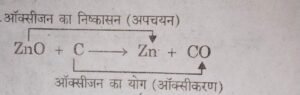
प्रश्न 9. N2 + 3H2 → 2NH3 में रासायनिक अभिक्रिया का प्रकार बताइए।
उत्तर- संयोजन अभिक्रिया।
प्रश्न 10. निम्नलिखित समीकरणों में अभिक्रिया के प्रकार की पहचान कीजिए-
(i) CuSO4+Zn → ZnSO4 + Cu
(ii) CaO+H₂O → Ca (OH)2
उत्तर- (i) विस्थापन अभिक्रिया है क्योंकि Zn, CuSO4 से Cu को विस्थापित कर रहा है।
(ii) संयोजन अभिक्रिया है क्योंकि CaO तथा H₂O के संयोग से केवल एक उत्पाद Ca (OH), बन रहा है।
प्रश्न 11. निम्नलिखित अभिक्रियाओं के सन्तुलित समीकरण लिखिए-
(i) हाइड्रोजन सल्फाइड गैस वायु में जलकर जल और सल्फर डाइऑक्साइड देती है।
(ii) बेरियम क्लोराइड का जलीय विलयन जिंक सल्फेट से क्रिया करके जिंक क्लोराइड और बेरियम सल्फेट देता है।
उत्तर-
(1) 2H2S+302 →2H₂O+2SO2
(ii) BaCl₂ +ZnSO4 → BaSO4 + ZnCl2
प्रश्न 12. विकृतगन्धिता से क्या तात्पर्य है? खाद्य पदार्थों की विकृत गन्धिता रोकने के दो उपाय बताइए।
उत्तर- विकृतगन्धिता (Rancidity)- वह प्रक्रिया जिसमें वायु की ऑक्सीजन द्वारा ऑक्सीकृत हो जाने से खाद्य पदार्थों के स्वाद एवं गन्ध में परिवर्तन हो जाता है, विकृतगन्धिता कहलाती है।
विकृतगन्धिता को रोकने के उपाय-
(i) खाद्य पदार्थों की वायुरोधी (air-tight) बर्तनों में रखा जाना चाहिए।
(ii) थैली (bags) में रखे आलू चिप्स को ऑक्सीकरण से बचाने के लिए थैली की वायु को नाइट्रोजन गैस से विस्थापित कर देना चाहिए।
प्रश्न 13. निम्नलिखित उदाहरणों में रासायनिक अभिक्रियाओं के प्रकार बताइए-
(i) पेट में भोजन का पचना,
(ii) कोयले का वायु में जलना,
(iii) लोहे पर जंग लगना,
(iv) तनु HCI की NaOH के साथ क्रिया से सोडियम क्लोराइड तथा जल बनना।
उत्तर-
(i) अपघटन अभिक्रिया, (ii) संयोजन या योगात्मक अभिक्रिया, (
iii) ऑक्सीकरण अभिक्रिया, (iv) उदासीनीकरण अभिक्रिया।
प्रश्न 14. निम्न रासायनिक समीकरण को सन्तुलित कीजिए-
![]()
उत्तर-![]()
प्रश्न 15. रासायनिक समीकरण को किस आधार पर संतुलित किया जाता है?
उत्तर- रासायनिक समीकरण को तत्त्वों के परमाणुओं को गिनकर संतुलित किया जा सकता है।
प्रश्न 16. निम्नलिखित अभिक्रियाओं का संतुलित रासायनिक समीकरण लिखिए-
(i) जिंक + सिल्वर नाइट्रेट = जिंक नाइट्रेट + सिल्वर
(ii) मैग्नीशियम + हाइड्रोजन क्लोराइड = मैग्नीशियम क्लोराइड + हाइड्रोजन
उत्तर-
(i) Zn+ 2AgNO3 → Zn(NO₃)₂ + 2Ag
(ii) Mg + 2HCl → MgCl₂ + H₂
प्रश्न 17. रेडॉक्स अभिक्रिया को एक उदाहरण द्वारा समझाइए।
उत्तर- वह रासायनिक अभिक्रिया जिसमें एक अभिकारक का ऑक्सीकरण तथा दूसरे अभिकारक का अपचयन होता है, रेडॉक्स अभिक्रिया या उपचयन-अपचयन अभिक्रिया कहलाती है।.
उदाहरण-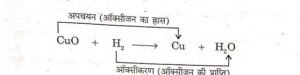
प्रश्न 18. निम्न रेडॉक्स अभिक्रियाओं में ऑक्सीकारक तथा अपचायक चुनिए-
(i) 2H₂S + SO2 → 3S + 2H₂O
(ii) I2 + H₂ S → S + 2HI
उत्तर- (i) H₂S का ऑक्सीकरण हो रहा है अतः यह अपचायक है तथा SO2 का अपचयन हो रहा है अतः यह ऑक्सीकारक है।
(ii) H₂S का ऑक्सीकरण हो रहा है अतः यह अपचायक है तथा I2 का अपचयन हो रहा है अतः यह ऑक्सीकारक है।
प्रश्न 19. दहन तथा संकलन अभिक्रिया पर संक्षिप्त टिप्पणी लिखिए।
उत्तर- दहन अभिक्रिया (Combustion Reaction)- वह रासायनिक अभिक्रिया जिसमें कोई पदार्थ वायु (ऑक्सीजन) की उपस्थिति में जल जाता है अथवा ऑक्सीकृत हो जाता है दहन अभिक्रिया कहलाती है।
उदाहरणार्थ: LPG के प्रमुख घटक ब्यूटेन (C4H10) का दहन निम्नवत् होता है-
C4H10(g)+ 13/2 O2(g) → 4 CO₂(g) + 5 H₂O (l)
संकलन अभिक्रिया (Addition Reaction)- वह रासायनिक अभिक्रिया जिसमें दो या दो से अधिक पदार्थ (तत्त्व या यौगिक) संयोग करके एकल उत्पाद का निर्माण करते हैं संकलन या योगात्मक अभिक्रिया कहलाती है।
उदाहरणार्थ :![]()
लघु उत्तरीय प्रश्न
प्रश्न 1. संयोजन अभिक्रियाओं से आप क्या समझते हैं? दो उदाहरणों द्वारा समझाइए।
उत्तर- वह अभिक्रियाएँ जिनमें दो या दो से अधिक पदार्थ संयोजित होकर एक पदार्थ बनाते हैं, संयोजन अभिक्रियाएँ कहलाती हैं।
उदाहरण– 
प्रश्न 2. ऊष्माक्षेपी तथा ऊष्माशोषी अभिक्रियाएँ क्या हैं?
अथवा ऊष्माक्षेपी रासायनिक अभिक्रिया को उदाहरण द्वारा समझाइए।
उत्तर- ऊष्माक्षेपी अभिक्रियाएँ- ऐसी अभिक्रियाएँ जिनमें ऊर्जा का उत्सर्जन होता है, ऊष्माक्षेपी अभिक्रियाएँ कहलाती हैं।
उदाहरण- मेथेन गैस का वायु में जलना
![]()
ऊष्माशोषी अभिक्रियाएँ– ऐसी अभिक्रियाएँ जिनमें ऊर्जा का अवशोषण होता है ऊष्माशोषी अभिक्रियाएँ कहलाती हैं। मरक्यूरिक ऑक्साइड का ऊष्मीय वियोजन।
उदाहरण-![]()
प्रश्न 3. द्विविस्थापन अभिक्रिया क्या है? एक उदाहरण देकर समझाइए।
उत्तर- वह अभिक्रिया जिसमें यौगिकों के आयनों अथवा परमाणुओं के समूहों की परस्पर अदला-बदली (विनिमय) हो जाता है, द्विविस्थापन अभिक्रिया कहलाती है।
उदाहरण-![]()
इस अभिक्रिया में Na तथा Ag आयनों का विनिमय होता है।
प्रश्न 4. लेड (II) नाइट्रेट तथा पोटैशियम आयोडाइड के विलयन परस्पर मिलाए जाते हैं-
(i) प्राप्त अवक्षेप का रंग क्या है तथा अवक्षेप का नाम बताइए।
(ii) इस अभिक्रिया के लिए सन्तुलित रासायनिक समीकरण लिखिए।
(iii) यह किस प्रकार की अभिक्रिया है?
उत्तर- (i) प्राप्त अवक्षेप का रंग पीला है। यह अवक्षेप लेड आयोडाइड है।
(ii)![]()
(iii) यह द्विविस्थापन अभिक्रिया है।
प्रश्न 5. (i) क्या होता है जब तनु हाइड्रोक्लोरिक अम्ल सोडियम कार्बनिट में मिलाया जाता है?
(ii) क्या होता है जब जिंक चूर्ण को तनु सल्फ्यूरिक अम्ल में मिलाया जाता है?
उपर्युक्त अभिक्रिया के लिए रासायनिक समीकरण लिखिए।
उत्तर- (ⅰ) जब तनु हाइड्रोक्लोरिक अम्ल सोडियम कार्बोनेट में मिलाया जाता है तो कार्बन डाइऑक्साइड गैस उत्पन्न होती है।

प्रश्न 6. रेडॉक्स अभिक्रिया किसे कहते हैं? अभिक्रिया, ZnO + C → Zn + CO में किस पदार्थ का उपचयन एवं किसका अपचयन हो रहा है?
अथवा
क्या उपचयन (ऑक्सीकरण) अथवा अपचयन अकेले हो सकते हैं? क्यों और क्यों नहीं? ऐसी अभिक्रियाओं को क्या कहते हैं?
उत्तर- रेडॉक्स अभिक्रियाएँ– वे रासायनिक अभिक्रियाएँ जिनमें ऑक्सीकरण (उपचयन) तथा अपचयन दोनों अभिक्रियाएँ साथ-साथ होती हैं, रेडॉक्स अभिक्रियाएँ कहलाती हैं।
किसी रासायनिक अभिक्रिया में एक अभिकारक ऑक्सीकृत (उपचयित) तथा दूसरा अभिकारक अपचयित होता है अतः उपचयन अथवा अपचयन क्रिया अकेले सम्भव नहीं है। उदाहरणार्थ-
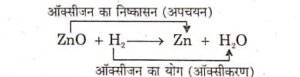
स्पष्ट हैं कि उपर्युक्त अभिक्रिया में ZnO का Zn में अपचयन तथा H2 का H₂O में ऑक्सीकरण हो रहा है अर्थात् ऑक्सीकरण तथा अपचयन अभिक्रियाएँ साथ-साथ होती हैं।
प्रश्न 7. विस्थापन और द्विविस्थापन अभिक्रियाओं में तीन अन्तर बताइए। प्रत्येक का एक-एक उदाहरण दीजिए।
उत्तर- विस्थापन एवं द्विविस्थापन अभिक्रियाओं में अन्तर
|
विस्थापन अभिक्रियाएँ |
द्विविस्थापन अभिक्रियाएँ |
| 1. वे अभिक्रियाएँ जिनमें किसी यौगिक में उपस्थित एक तत्त्व का स्थान कोई दूसरा तत्त्व ले लेता है, विस्थापन या प्रति- स्थापन अभिक्रियाएँ कहलाती हैं।
जैसे-CuSO4 + Fe → FeSO4 + Cu 2. इस प्रकार की अभिक्रियाएँ आयनिक प्रकृति की नहीं होती हैं। 3. ये एकल विस्थापन अभिक्रि- याएं हैं। |
1. वे अभिक्रियाएँ जिनमें अभिकारकों के आयनों का विनिमय (अदला- बदली) होता है, द्विविस्थापन अभिक्रियाएँ कहलाती है।
जैसे- AgNO3 + NaCl → AgCl + NaNO3 2. ये अभिक्रियाएँ आयनिक प्रकृति की होती हैं। 3. ये द्विविस्थापन अभिक्रियाएँ हैं। |
प्रश्न 8. जिंक की सल्फ्यूरिक अम्ल से क्रिया होने पर गैस X बनती है-
(a) गैस X का नाम दीजिए।
(b) अभिक्रिया का समीकरण लिखिए।
(c) गैस X की पहचान कैसे करेंगे?
उत्तर- (a) गैस X = हाइड्रोजन गैस।
(b) Zn(s) + H₂SO₄(aq) → ZnSO4 (aq) + H2↑
(c) हाइड्रोजन गैस की पहचान– गैस में भरी परखनली के मुख पर जलती हुई मोमबत्ती ले जाने पर यदि गैस ‘फट ध्वनि’ (pop sound) करके जलती है, तो वह हाइड्रोजन गैस है।
प्रश्न 9. योगात्मक अभिक्रिया तथा प्रतिस्थापन अभिक्रिया को एक-एक उदाहरण द्वारा समझाइए।
अथवा
कार्बनिक यौगिकों में योगात्मक तथा प्रतिस्थापन अभिक्रियाओं को एक-एक उदाहरण देकर स्पष्ट करें।
उत्तर- योगात्मक (संयोजन) अभिक्रिया वह रासायनिक अभिक्रिया, जिसमें दो या दो से अधिक पदार्थ, तत्त्व या यौगिक संयोग करके एकल उत्पाद का निर्माण करते हैं, संयोजन अभिक्रिया कहलाती है।
उदाहरण- ![]()
प्रतिस्थापन अभिक्रिया वह रासायनिक अभिक्रिया, जिसमें अधिक क्रियाशील तत्त्व कम क्रियाशील तत्त्व के यौगिक से उस तत्त्व के परमाणु को विस्थापित कर स्वयं उसका स्थान ग्रहण कर लेता है, प्रतिस्थापन अभिक्रिया कहलाती है।
उदाहरण-![]()
प्रश्न 10. वियोजन अभिक्रिया क्या है? एक उदाहरण दीजिए।
उत्तर- वह अभिक्रिया जिसमें एक यौगिक वियोजित होकर दो या दो से अधिक पदार्थों में परिवर्तित हो जाता है, वियोजन अभिक्रिया कहलाती है।
उदाहरण – ![]()
प्रश्न 11. ऊष्मीय वियोजन क्या है?
उत्तर- जब एक वियोजन अभिक्रिया में अभिकारकों को गर्म करने पर उत्पाद प्राप्त होते हैं तो वह अभिक्रिया उष्मीय वियोजन कहलाती है।
उदाहरण- ![]()
प्रश्न 12. शरीर में भोजन का पाचन किस प्रकार की अभिक्रिया है? स्पष्ट कीजिए।
उत्तर- शरीर में भोजन का पाचन वियोजन अभिक्रिया है। जब हम चावल, गेहूँ या आलू खाते हैं तब इन पदार्थों से प्राप्त स्टार्च का शर्करा में तथा प्रोटीन का ऐमीनो अम्लों में वियोजन हो जाता है।
प्रश्न 13. ऊष्मीय वियोजन और आयनिक वियोजन में अन्तर लिखिए।
उत्तर- ऊष्मीय वियोजन और आयनिक वियोजन में अन्तर
|
ऊष्मीय वियोजन |
आयनिक वियोजन |
| 1. ऊष्मीय वियोजन ऊष्मा के द्वारा होता है। | 1. आयनिक वियोजन विलयन बनाने पर होता है। |
| 2. ऊष्मीय वियोजन में उत्पाद उदासीन अणु होते हैं। | 2. आयनिक वियोजन में उत्पाद आयन होते हैं। |
| 3. ऊष्मीय वियोजन में उत्पाद पृथक किये जा सकते हैं। | 3. आयनिक वियोजन के उत्पाद पृथक नहीं किये जा सकते। |
| 4.ऊष्मीय वियोजन के लिये माध्यम आवश्यक नहीं है। | 4. आयनिक वियोजन के लिए माध्यम आवश्यक नहीं है। |
प्रश्न 14. निम्नलिखित में से कौन-से परिवर्तन ऊष्माशोषी और कौन-से ऊष्माक्षेपी प्रकृति के हैं-
(a) फेरस सल्फेट का अपघटन
(lb) सल्फ्यूरिक अम्ल का तनुकरण
(c) सोडियम हाइड्रॉक्साइड का जल में विलीन होना
(d) अमोनियम क्लोराइड का जल में विलीन होना।
उत्तर- (b) तथा (c) ऊष्माक्षेपी हैं क्योंकि इन परिवर्तनों में ऊष्मा मुक्त होती है।
(a) तथा (d) ऊष्माशोषी हैं, क्योंकि इन परिवर्तनों में ऊष्मा अवशोषित होती है।
प्रश्न 15. निम्नलिखित समीकरणों को संतुलित कीजिए-
(i) H2 + Br2 → HBr
(ii) Na+ O2→ Na2O
(iii) P+O2 → P205
(iv) CO+O2 → CO2
(v) NaOH + H2SO4 → Na2SO4 + H2O
उत्तर- (i) H2 + Br2 → HBr
H तथा Br के परमाणुओं की संख्या दोनों ओर समान करने के लिए HBr में 2 से गुणा करने पर
H2 + Br2 → 2HBr
Na + 02 → Na2O
(ii) 0 की संख्या समान करने के लिए दाहिनी ओर 2 का गुणा करने पर
Na+ O2 → 2 Na₂O
अब Na की संख्या समान करने के लिए Na में 4 का गुणा करने पर
4 Na + O2 → 2Na2O
अथवा
0 के 1 परमाणु से Na के दो परमाणु संयोग करके 1 अणु Na2O बनाते हैं। अतः बायीं ओर के 2 परमाणुओं से संयोग हेतु Na के 4 परमाणु चाहिए तथा इससे 2 अणु Na2O के बनेंगे। अतः
4Na + O2 → 2Na2O
P + O2 → P205
(iii) P205 सूत्र के P के 2 परमाणुओं से O के 5 परमाणु संयोग करते हैं। अतः P के 2 परमाणु लेने पर O के 5 परमाणु या 21/2 अणु लेने होंगे। तदनुसार 2P+21/2 O →P2O5
परन्तु 1/2 अणु का कोई अर्थ नहीं है-अतः पूरे समीकरण में 2 का गुणा करने पर
4P + 502 → P205
CO + O2 → CO2
(iv) चूँकि का एक परमाणु CO के एक अणु से संयोग करके CO₂ बनाता है, O के दो परमाणु (O2), से CO के दो अणु संयोग करके 2 अणु CO₂ बनायेंगे। अतः
2CO+O2 → 2CO2
NaOH + H2SO4 → Na2SO4 + H2O
(v) Na परमाणुओं की संख्या के संतुलन हेतु बायीं ओर NaOH के 2 अणु होने चाहिए। तदनुसार
2 NaOH + H2SO4 → Na2SO4 + H2O अब H परमाणुओं की संख्या के संतुलन हेतु दाहिनी ओर H2O के दो अणु होने चाहिए-अतः
2NaOH + H2SO4 → Na2SO4+ 2H2O